Los efectos de la calidad del agua en la agricultura de riego
Allan Huysamen
Introducción
El agua es un excelente solvente para moléculas polares y especies cargadas, incluyendo aniones y cationes inorgánicos simples. En consecuencia, cuando el agua interactúa con depósitos minerales, suelos, rocas o material orgánico, las especies se solubilizan dentro del agua, definiendo las propiedades del agua. La idoneidad de una fuente de agua para uso en riego, y sus efectos subsecuentes en la salud del suelo y de los cultivos, dependen en gran medida de la concentración e identidad de iones inorgánicos disueltos. Esto debe entenderse para poder gestionar el agua de manera eficaz.
Factores que afectan la idoneidad del agua
La idoneidad del agua para riego depende de varios factores, entre ellos la salinidad, el peligro de sodio, las concentraciones de cationes nutrientes, las concentraciones de iones metálicos, el pH, la alcalinidad y los iones inductores de toxicidad. Estos factores, sus respectivos efectos en la idoneidad del agua y la forma en como pueden gestionarse, requieren un análisis más detallado.
Salinidad
El contenido total de sales disueltas, representado convenientemente por la medición de la conductividad eléctrica (CE), nos permite conocer la concentración total de iones disueltos en el agua. Irrigar con agua con un contenido muy bajo de sales disueltas (CE < 0,4 mS.cm-1) puede contribuir a la lixiviación de iones de la capa superior del suelo, a la dispersión de las partículas del suelo y a una reducción definitiva de la capacidad de infiltración de agua. Por otro lado, las fuentes de agua con un alto contenido de sales disueltas (CE > 0,75 mS.cm-1) depositarán iones en exceso en el perfil del suelo, lo que resultará en un efecto acumulativo con cada ciclo de riego y a medida que el agua se elimina por evapotranspiración o evaporación superficial. Una mayor concentración de iones en la zona de las raíces alterará el potencial osmótico de la solución de agua del suelo y, eventualmente, conducirá a una reducción en el agua disponible para las plantas. En suelos bien drenados, se puede emplear una estrategia de lixiviación para reducir el contenido de sal de la solución del suelo, aplicando periódicamente agua en exceso para empujar las sales por debajo de la zona de las raíces.
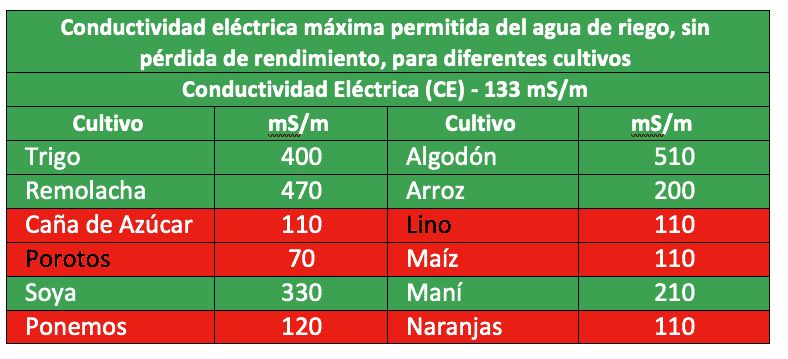
Diferentes cultivos tienen diferentes niveles de tolerancia a la salinidad en relación con la CE del agua de riego. Debe evitarse el uso de agua de alta salinidad en cultivos con baja tolerancia a la salinidad, especialmente si la lixiviación no es posible debido a un drenaje deficiente o a una disponibilidad de agua inadecuada. Comprender la tolerancia a la salinidad de sus cultivos en relación con la salinidad de su agua de riego, como se proporciona y se muestra en el Informe de Riego de Agri Technovation ITEST™ WATER (Tabla 1), es importante para tomar decisiones sobre el uso de la fuente de agua para el riego.
Tabla 1: Extracto de un Informe de Riesgo – ITEST™ WATER, que muestra el valor CE analizado junto con los valores umbral de CE para varios cultivos, por encima de los cuales se espera una pérdida potencial de producción.
Relación de Absorción de Sodio (RAS)
El RAS es el valor calculado, que caracteriza la abundancia de iones de sodio en relación con los iones de calcio y magnesio en el agua. El agua con un valor alto de RAS indica que los iones de sodio están presentes en una concentración desproporcionadamente alta, lo que probablemente resultará en una mayor representación de sodio en los coloides del suelo. Además de los efectos nutricionales de un alto porcentaje de sodio intercambiable, la dominancia de sodio en los coloides del suelo puede conducir a la dispersión de partículas del suelo. Esto podría llevar a la degradación de la estructura del suelo, lo que provocará una infiltración deficiente del agua, un aumento de la compactación y una reducción del contenido de oxígeno en la zona de las raíces, lo que afectará negativamente la prosperidad y la productividad del cultivo. Sin embargo, el suelo puede remediarse con mejoradores como el yeso, que suministra cationes de calcio para desplazar el sodio de los coloides del suelo, y aniones de sulfato para facilitar la lixiviación de iones de sodio desplazados.
Se debe evitar el agua con un SAR alto (> 10) en suelos de textura fina con una alta capacidad de intercambio catiónico (CIC), mientras que incluso valores moderados de SAR (> 3) pueden requerir la aplicación relativamente constante de mejoradores para preservar la estructura del suelo.
Cationes Nutrientes
Las proporciones y concentraciones de cationes nutritivos como potasio, magnesio y calcio también son significativas. Una alta concentración de potasio en las fuentes de agua es poco frecuente y suele sugerir una fuente de agua contaminada con fertilizantes. El potasio en altas concentraciones puede interferir con la captación de otros iones, como el magnesio. Además, una concentración desproporcionadamente alta de magnesio puede tener un efecto similar al del sodio en la integridad de la estructura del suelo, lo que puede causar problemas de infiltración y promover la formación de terrones de suelo indeseables.
Iones metálicos
Aunque ciertos iones metálicos son necesarios para la nutrición de las plantas, pueden ser problemáticos en ciertas concentraciones y bajo ciertas condiciones. En general, los iones metálicos presentan una mayor solubilidad y disponibilidad para su absorción en condiciones ácidas (pH < 7), lo que puede plantear problemas de toxicidad dependiendo de sus concentraciones. Por otro lado, en condiciones alcalinas (pH > 7), se promueve la oxidación y precipitación de iones metálicos, lo que puede provocar obstrucciones en sistemas de riego más finos. La concentración a la cual surge el potencial de toxicidad bajo condiciones ácidas varía según el metal (Tabla 2) y la sensibilidad específica del cultivo.1 El hierro y el manganeso también son en gran medida responsables de las obstrucciones en sistemas de riego fino bajo condiciones más alcalinas, especialmente cuando su concentración supera los 0,4 mg.L-1.
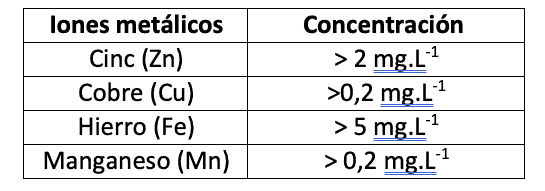
Tabla 2: Tabla de iones metálicos y las concentraciones correspondientes a las que el ion tiene potencial de toxicidad en condiciones ácidas.
La concentración de iones metálicos, especialmente hierro y manganeso, puede reducirse mediante oxidación química o aireación, seguida de filtración o sedimentación.
pH y Alcalinidad
El pH del agua rige el estado físico y la disponibilidad para la planta de los iones solubilizados en el agua, aunque se espera que el pH del agua se neutralice o equilibre en cierta medida al entrar en contacto con la solución amortiguadora del suelo. La máxima disponibilidad de los macronutrientes primarios y secundarios se alcanza en torno a un pH neutro, mientras que los micronutrientes se vuelven en gran medida más disponibles a medida que el pH tiende a 5. Sin embargo, un pH alcalino del agua estimulará la precipitación de sales de carbonato, como CaCO3, así de iones metálicos.
La alcalinidad de una fuente de agua depende directamente de la concentración de iones bicarbonato y carbonato en la fuente de agua, definiendo la capacidad de amortiguación del agua. Una baja alcalinidad (< 40 mg.L– 1 como CaCO3) hará que el agua sea susceptible a las fluctuaciones de pH, lo cual es particularmente importante considerar durante la fertirrigación. Una alta alcalinidad (> 90 mg.L-1 como CaCO3) hará que el agua resista la acidificación y que promueva la precipitación de CaCO3 y otras sales carbonatadas. Irrigar con agua de alta alcalinidad puede causar problemas operativos, incluyendo la deposición de CaCO3 en los sistemas de riego, lo que finalmente conduce a obstrucciones. Además, se ha informado que el uso de agua altamente alcalina causa trastornos nutricionales al interferir con la absorción y translocación de ciertos iones, incluyendo el calcio y el hierro.2
El agua de alta alcalinidad puede ser corregida mediante una estrategia de acidificación, que actúa para neutralizar las especies de carbonatos y bicarbonatos en el agua y así reducir la alcalinidad a un nivel más favorable. Esto se puede lograr mediante la aplicación de fertilizantes ácidos en el agua, o mediante la inyección de ciertos ácidos a una tasa calculada.
Iones Inductores de Toxicidad
Ciertos iones tendrán un efecto tóxico en los cultivos cuando estén presentes por encima de sus respectivas concentraciones umbral. Esto conducirá eventualmente a la pérdida de potencial de producción. Los iones que pueden causar un efecto tóxico incluyen el boro y el cloruro, ambos necesarios para la nutrición de las plantas en concentraciones más bajas. En exceso y a medida que las concentraciones en el agua de riego aumentan, eventualmente causarán clorosis, necrosis y pérdida de potencial fotosintético. La gravedad de la respuesta de toxicidad para una concentración dada de cloruro o boro es específica del cultivo, siendo generalmente los cultivos de frutas y frutos secos los mas sensibles. La eliminación de cloruro y boro del agua de riego no suele ser factible, por lo que la mezclar fuentes de agua es una de las únicas soluciones prácticas para reducir la concentración de ambos iones en el agua de riego.
Tener conocimiento de la concentración de iones inductores de toxicidad en sus fuentes de agua de riego y comprender la tolerancia de sus cultivos hacia estos iones es extremadamente importante para la selección y manejo de las fuentes de agua. Junto con las concentraciones analizadas proporcionadas en el Informe de Riego – ITEST™WATER de Agri Technovation, se destacan las sensibilidades específicas de los cultivos para prevenir los problemas de toxicidad (Figura 1).
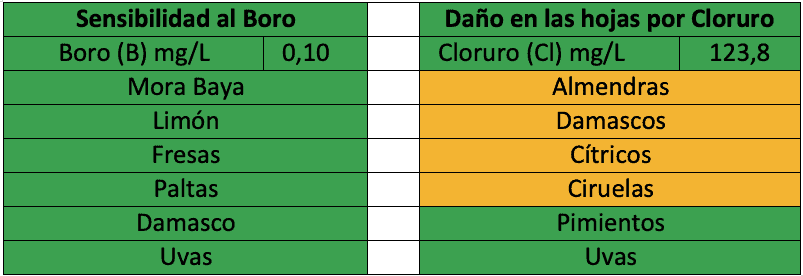
Figura 1: Extracto de un Informe de Análisis de Riego – ITEST™WATER, que muestra las concentraciones de cloruro y boro analizadas y destaca la sensibilidad de los cultivos a las concentraciones analizadas.
Una solución: ITEST™WATER – Análisis de Riego
El servicio de Análisis de Riego ITEST™WATER de Agri Technovation tiene como objetivo proporcionar la información más importante necesaria para evaluar la idoneidad de una fuente de agua para su uso de riego. Los datos del análisis se muestran en un formato gráfico para facilitar la interpretación (Figura 2), teniendo en cuenta también las sensibilidades específicas del cultivo cuando corresponda. Esto permite identificar con relativa rapidez los posibles problemas y comparar entre diversas fuentes de agua, así como resaltar los casos en que puede ser necesario aplicar estrategias de gestión. El análisis periódico de una única fuente de agua también es importante para monitorear los cambios en la calidad del agua a lo largo del tiempo, ya que los cambios ocurren a corto plazo debido a la sequía o a precipitaciones excesivas, y a largo plazo debido a factores antropogénicos y al cambio climático.
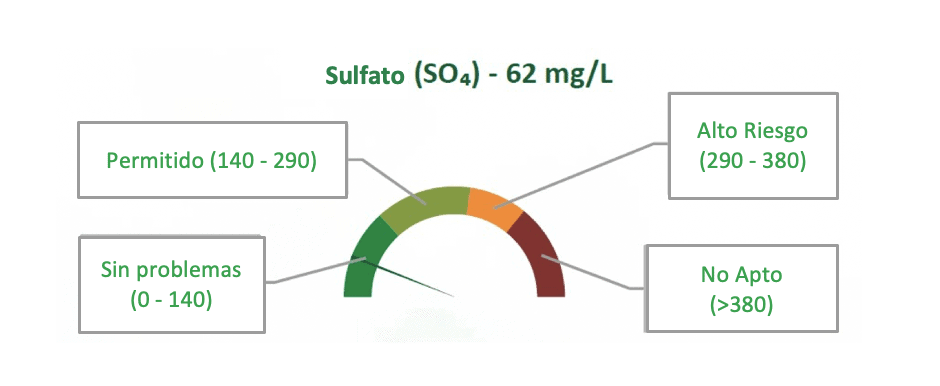
Figura 2: Un gráfico como este se proporciona en el Informe de Riesgo – ITEST™WATER, el cual muestra la concentración de sulfato analizada y los límites asociados para determinar su idoneidad.
Referencias
- S. Ayers y D.W. Westcot, Water Quality for Agriculture, FAO, Roma, 1985.
- Shahabi, M.J. Malakouti y E. Fallahi, J. Plant Nutr., 2005, 28, 1663-1678.

